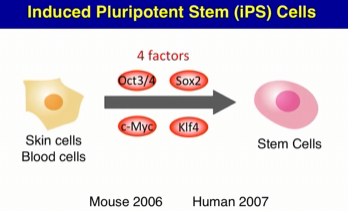
Yamanka 인자는 세포를 불소능 배아 줄기 세포로 재프로그램하며,
4가지 프로그래밍 인자(Oct4, Sox2, Klf4 및 c-Myc(OSKM))만 사용하여 세포의 세포 정체성을 재설정합니다(따라서 세포는 자신의 기능과 예정된 기관을 잊어버립니다). 충분한 시간 동안 재프로그래밍 인자에 노출되면 정체성을 지우지 않고 세포의 나이를 되돌릴 수 있습니다.
이것은 부분적인 세포 재프로그래밍의 기초입니다.
Nature에 발표된 연구에서 과학자들은 이것이 신경 발생, 즉 새로운 뉴런 생성에 미치는 영향을 보고합니다.
신경 아세포 생성 증가.
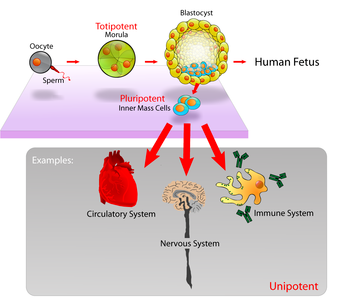
오래된 뇌가 새로운 뉴런을 생성하지 않는다는 일반적인 오해가 있던 시대는 이미 지났습니다.
그 이후로 과학자들은 해마 및 뇌실하대(SVZ)와 같은 뇌의 특정 영역에
성인이 되어도 새로운 뉴런을 발생시키는 신경성 틈새가 포함되어 있음을 발견했습니다.
그러나 이 과정은 나이가 들수록 상당히 느려집니다.
연구에서 연구원들은 고전적인 Yamanaka OSKM 칵테일을 사용했습니다.
많은 연구자들이 재프로그래밍의 효율성을 높이고 주로 c-Myc과 관련된 종양인 종양의 위험을 낮추는 방법에 관심을 가져왔지만 이번 연구에서는 그렇지 않았습니다.
먼저 과학자들은 분자 유발 인자(이 경우에는 독시사이클린)로 치료할 때 OSKM을 발현하는 유전자 조작 쥐를 만들어 전신 재프로그램을 진행했습니다.
단일 세포 RNA 시퀀싱을 사용하여 연구자들은 나이가 들수록 신경줄기세포(NSC)의 후손 중에서 뉴런의 바로 전구체인 신경모세포의 비율이 감소하여 신경 발생이 손상되었음을 나타냅니다.
치료는 이러한 추세를 역전시켜 신경모세포의 비율을 젊은 수준으로 되돌렸습니다.
다음으로, 연구원들은 OSKM 발현이 공간적으로 SVZ로만 제한되는 훨씬 더 정교한 마우스 모델을 사용했습니다.
흥미롭게도 이러한 제한을 통해 OSKM의 표현 시간을 전신 모델에서 치명적인 수준까지 늘리고 안전하게 작업할 수 있었습니다.
NSC와 신경아세포에 대한 효과는 전신 재프로그래밍보다 훨씬 더 인상적이었습니다.
다시 프로그래밍된 뉴런 측정항목
틈새에 미치는 영향을 피하기 위해 연구원들은 시험관 내에서 배양된 NSC를 대상으로 실험도 수행했습니다.
살아있는 유기체와 마찬가지로 늙은 쥐에서 채취한 NSC는 어린 쥐에서 채취한 것보다 더 낮은 비율의 신경모세포를 생성했습니다.
OSKM으로 NSC를 치료하면 자손의 신경모세포 비율이 증가하여
'정상으로 돌아가는' 재생 유사 효과를 시사합니다.
그러나 우리가 궁극적으로 관심을 갖는 것은 신경모세포 전구체가 아니라 뉴런입니다.
치료로 인해 더 많은 뉴런이 탄생했습니까? 분명히 그렇습니다.
생쥐에서 SVZ 유래 신경아세포는 후각 영역으로 이동하여 성숙한 뉴런이 됩니다(이는 후각이 이 동물에게 얼마나 중요한지 보여줍니다).
나이가 들수록 이 과정은 급격히 느려집니다.
OSKM 치료는 후각구에서 생성되는 뉴런의 수를 증가시켰지만 청소년 수준까지는 아니었습니다.
단일 세포 전사 및 면역 염색 검증을 사용하여 우리는 노화된 쥐의 부분적인 전신 재프로그래밍이 SVZ 신경성 틈새에서 신경모세포 비율의 연령 관련 결함을 부분적으로 역전시키는 것을 발견했습니다.
이 "회춘" 효과는 SVZ 자체를 대상으로 부분 재프로그래밍을 통해 재현할 수 있으며 이는 본질적인 현상을 나타냅니다.
또한, 세포 배양에서 오래된 NSC의 부분 재프로그래밍은 신경 전구 세포로의 분화를 자율적으로 향상시킵니다.
문제의 연구는 여러 다른 세포 유형에 대한 효과를 체계적으로 테스트하여 오래된 뇌에서 부분 재프로그래밍의 효과를 보여줍니다.
전체 연구: